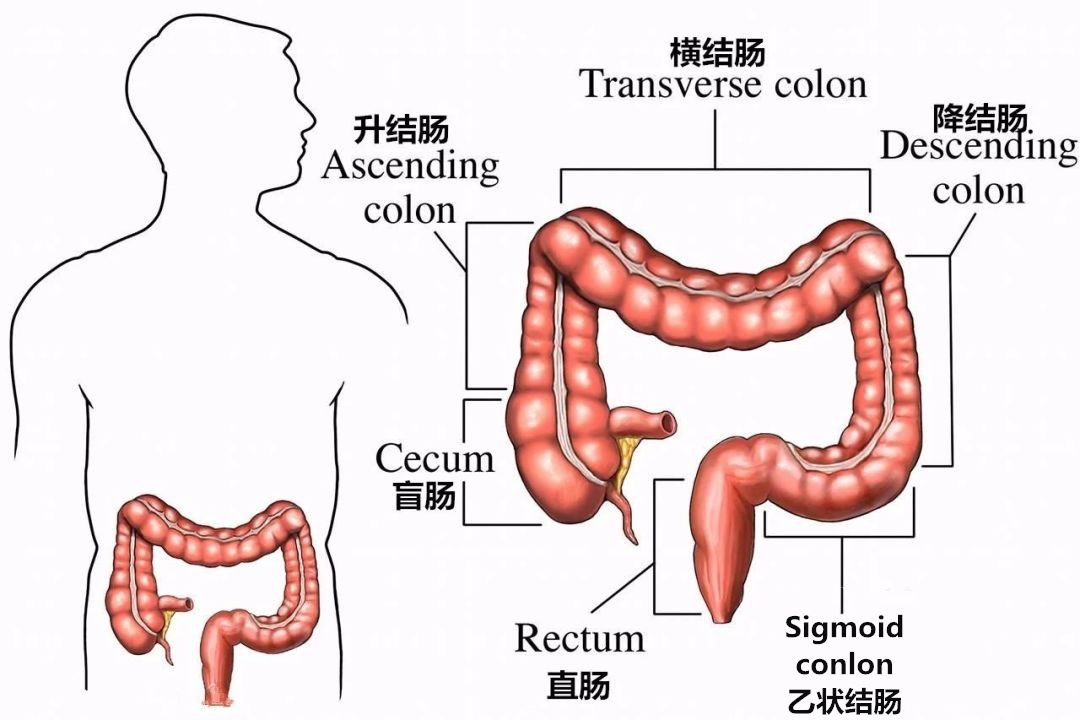
筛查不足,80%发现时已是晚期
尽管目前肠癌的总体治疗效果比较好,但由于目前我们缺乏系统性的结直肠癌筛查计划,加之普通人群对预防结直肠癌的意识不强,所以我们国家临床上发现的肠癌中晚期占80%以上,不但治疗费用高,而且治疗效果不理想。对于直肠癌,很多患者由于发现晚,不得不做肛门切除和结肠永久造瘘(改道),术后生活质量差。有的已经发生了局部和远处转移,治愈的机会就很小了。
肠癌该怎么治?
癌的治疗目前仍然是以手术为主,根据肿瘤侵犯肠管的深度和淋巴结转移的数目决定肠癌术后的分期,并根据临床分期是否需要辅助放化疗。
术前评估除常规全身检查和基本状态评估外,还要进行胸腹部增强CT检查,判断肿瘤情况及是否有淋巴结、肝脏和肺部转移,对于直肠癌可能还建议进行盆腔磁共振检查以评估肿瘤是否侵犯直肠系膜、肿瘤与肛提肌的距离,以判断保留肛门的可能性和是否需要术前新辅助治疗。
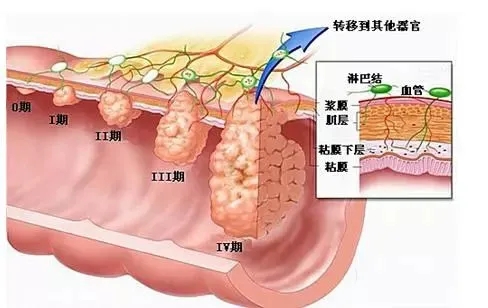
早中期肠癌的治疗策略
中晚期肠癌的治疗策略
研究显示,晚期肠癌患者达到切除或无瘤状态可长期生存。根据晚期肠癌患者的肿瘤负荷部位、大小、转移的数量等,可分为可切除、潜在可切除和不可切除种类型。1)对于可切除者,应选择合适的时机进行手术,使患者达到或状态,且在手术治疗期间应重视新辅助治疗和术后辅助治疗的合理应用;2)对于潜在可切除者,应通过转化治疗使肿瘤缩小、降期,转化为可切除病灶,化疗联合靶向治疗等方案能够患者通过转化治疗获得根治性切除,从而提高生存获益;3)对于不可切除者,应实施相对缓和的治疗方案,控制症状,改善生活质量,延长患者生存。树立全程管理的理念,通过多学科团队协作(MDT)制定个体化临床治疗方案,科学安排一线、二线及后线治疗,同时积极联合各种局部治疗手段以提高疾病的控制率、减轻肿瘤负荷,使患者生存获益最大化。
肠癌为什么要做基因检测?
指导靶向、免疫治疗用药
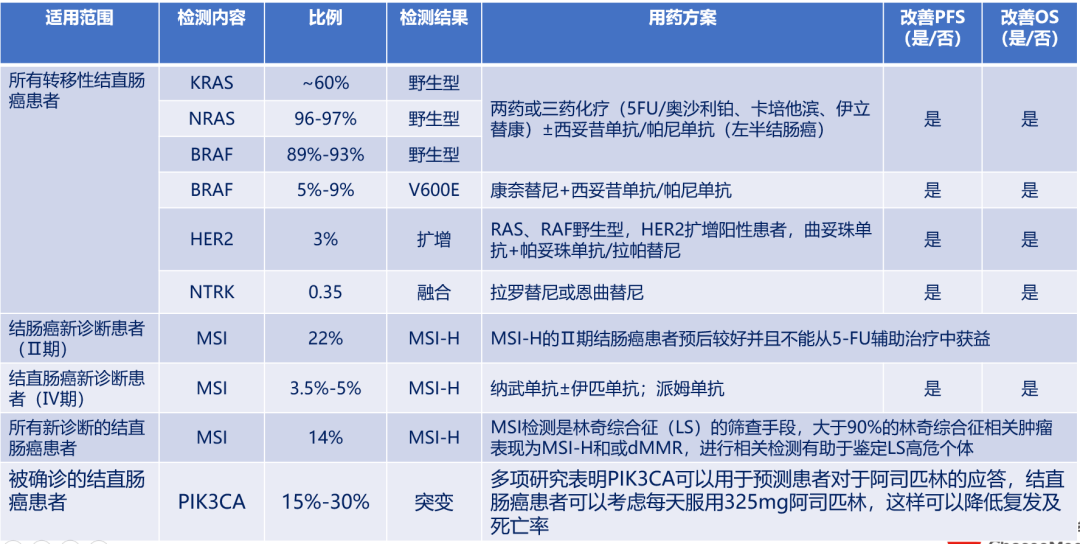
指导化疗用药
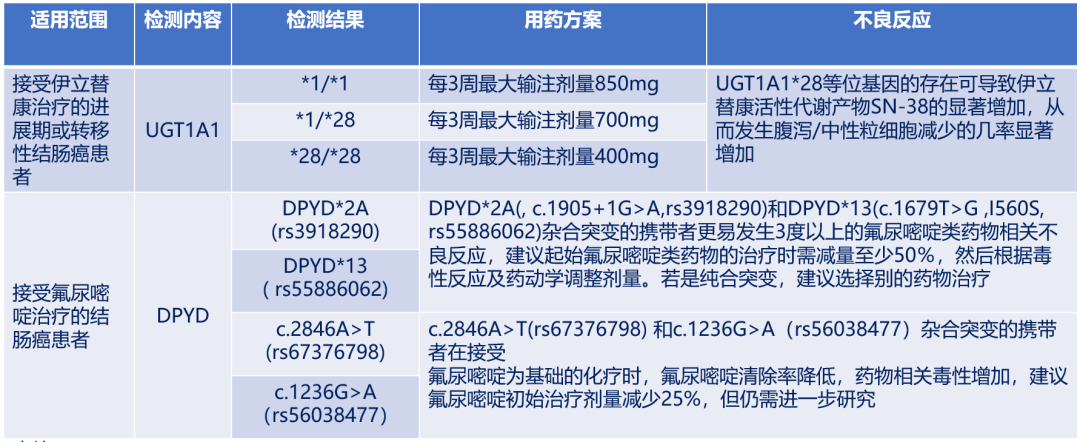
评估遗传风险
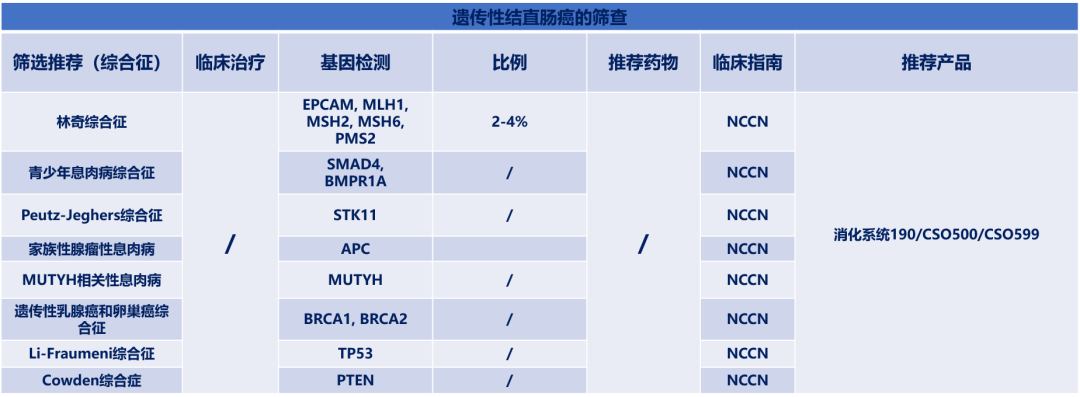
与遗传性结直肠癌相关的综合征有很多,以林奇综合征(LS)为例,该综合征由EPCAM, MLH1,MSH2, MSH6和PMS2的胚系致病性突变相关,患CRC等多种恶性肿瘤的风险增加,有这些基因突变导致的结直肠癌占总患者群体的2-4%。针对于LS个体,结肠癌的风险管理措施:从20-25岁开始进行结肠镜检查(如果是MSH6致病性突变,可以适当延迟结肠镜检查时间,比如从30岁开始,如果家族中有亲属罹患结肠癌需早于被确诊亲属发病年龄的10年开始结肠镜检查;PMS2的数据较少,暂时没有明确的结肠镜检查起始年龄推荐),如果最早的结肠癌患者早于25岁被确诊,建议早于确诊年龄的2-5年开始,每1-2年进行结肠镜检查(包含有结直肠癌家族史,性别为男性,携带MLH1/MSH2致病性突变,年龄大于40岁,有腺瘤史这些危险因素的个体更容易从每年的筛查中获益),有数据支持阿司匹林可以降低LS综合征患结肠癌的风险,但是合适的剂量和用药时间不明确。
总结
基于NGS的结直肠癌基因检测可以做到ALL IN ONE,一次检测提供多种提示信息:
1. 指导结直肠癌患者靶向药物选择,如靶向药西妥昔单抗只适用于KRAS、NRAS和BRAF野生型患者。
2. 指导结直肠癌患者免疫药物选择,如免疫治疗药物适合dMMR/MSI-H型患者。
3. 指导结直肠癌患者化疗药物选择,如UGT1A1*28等位基因的存在使得伊立替康毒副作用增加,因此应降低药物使用剂量。
4. 提示结直肠癌患者家族遗传风险,如携带MLH1基因胚系致病性突变个体,患结直肠癌风险增加,应加强筛查,早发现早治疗,争取最佳预后。

 新OA系统
新OA系统 汇联易
汇联易 企业邮箱
企业邮箱 旧OA系统
旧OA系统 DTMS系统
DTMS系统 CAPA系统
CAPA系统