
近日,首篇专注于儿科疾病的《宏基因组二代测序技术在新生儿感染性疾病中的临床应用专家共识》在《中华儿科杂志》发布。该共识由中华医学会儿科分会新生儿学组和中华儿科杂志编辑委员会撰写,国家儿童医学中心复旦大学附属儿科医院新生儿科周文浩教授为通信作者,基于国内外研究成果与专家经验,从mNGS技术的临床适应证、标本采集与转运、报告解读等方面给出建议。
该共识是国内第一个新生儿感染领域宏基因组学二代测序应用专家共识。其对于帮助儿科医生更合理、更规范地应用mNGS,提升mNGS在新生儿感染中应用的精准性有重要意义。

一、mNGS在NICU感染性疾病中的应用
共识1:
患儿具有急危重症表现,不除外感染, 或有继发或并发危及生命的严重感染,需要尽快明确病原体,建议常规检测的同时送检mNGS。
新生儿急危重症感染其致病微生物复杂,常规方法易遗漏部分病原微生物,因此建议常规检测的同时送检mNGS。多项研究表明mNGS对败血症的检测灵敏度远远高于传统培养。亦有研究通过检测败血症患者血浆样本的细胞游离DNA,表明基于mNGS 的检测结果有53%的患者治疗方案进行了调整。
共识2:
高度怀疑患儿存在新生儿血流感染甚至败血症时,若经验治疗 3 d效果不佳且常规微生物学检查送检阴性,建议调整经验抗微生物治疗方案的同时采集血液样本送检mNGS。推荐DNA测序作为血流感染的首选检测方法,在高度怀疑RNA病毒感染的情况下可同时进行RNA测序。
由于大部分血流感染的病原体(包括细菌、真菌、寄生虫、DNA病毒)均以DNA作为遗传物质,如果根据适应证送检 mNGS,推荐 DNA 测序作为血流感染的首选检测方法。但也应根据临床流行病学,如发病季节、母亲疾病史、生后时间及临床表现共同判断,选择进行DNA或RNA测序。
共识3:
对于疑似中枢神经系统(central nervous system,CNS)感染的患儿,条件允许的情况下建议留取常规、生化及微生物检查所需脑脊液的同时留取 mNGS 所需脑脊液,若脑脊液检查结果提示常规和(或)生化指标异常且常规微生物检测阴性且经验性抗感染治疗 3 d无效,建议立即送检mNGS。
脑脊液常规微生物检查的阳性率较其他类型样本低且脑脊液样本所含人核酸含量较低,因此脑脊液较适合开展mNGS检测。在测序方法的选择上,若临床排除病毒感染的可能,优先进行 DNA 测序。当脑脊液常规、生化无明显异常且脑脊液微生物学检查阴性,临床上仍高度怀疑 CNS 感染,或临床表现复杂、无特定怀疑方向送检 mNGS 时,推荐对脑脊液样本DNA和RNA同时进行测序。
共识4:
对于疑似呼吸道感染的重症患儿,常规微生物检查(培养或核酸检测)阴性且治疗3 d无效,可送检mNGS,应同时进行DNA及RNA测序。样本类型优先选择肺泡灌洗液,其次考虑气管插管下获得痰液及鼻咽拭子样本。
mNGS 可对包括呼吸道定植菌群和引起感染的病原菌同时进行检测,同时对于多重感染的鉴定具有极大优势;在传统病原微生物检测(包括培养、PCR等)阴性及免疫功能抑制的患儿中应用价值更高。
共识5:
疑似新发病原体、临床上提示可能有一定的传染性,或者疑似特殊病原体或罕见病原感染,常规微生物检测方法阴性,建议尽快完善mNGS。
mNGS具有检测新发病原和罕见病原的能力,但对于新发病原,由于缺乏参考基因组,完整的鉴定种属以及和已知种属的进化关系,需要较高的测序序列数,建议优先采集病灶标本或进行富集。
共识6:
疑似存在混合感染,常规微生物检查结果不能解释临床表现的全貌或抗感染治疗的反应,经验性治疗3 d无效时,建议进一步完善常规检测的基础上,开展mNGS。
相比于常规方法有限的检测范围,mNGS的原理使得其具有更广泛的检测范围,理论上可以检测任意病原微生物。这一特点使得其更易检出混合感染。已有研究表明对于肺部混合感染的检测,mNGS的灵敏度达到97.2%,而常规方法仅为13.9%。
共识7:
出现某种感染性疾病的聚集性发病或者疑似院内感染暴发,在常规快速检测不能明确病原时,建议开展mNGS。
mNGS 能够通过重构病原微生物间的亲缘关系,并结合流行病学信息,鉴定传播簇以及传播链,具有鉴定、监控传染性疾病的暴发和院内感染的能力。
共识8:
疑似局部感染,如眼部(角膜炎或溃疡、眼内炎、急性视网膜坏死等)、鼻部、耳部或局部蜂窝织炎等,在常规微生物检测未能明确病原情况下,可开展mNGS。
共识9:
由于各种原因导致的胸腔积液及腹腔积液,在送检常规生化及培养的同时留取胸、腹腔积液样本,若常规、培养阴性或经验性抗感染治疗3 d 无效 ,仍怀疑感染所致者 ,建议立即送检mNGS。
共识10:
对于 mNGS 检测阴性但临床高度怀疑感染的患儿,必要时再次取样复查mNGS。
共识11:
对常规微生物学检查容易明确病原体且经验治疗通常有效的感染,不建议常规进行mNGS 检测。不建议应用 mNGS 评估抗感染治疗效果。
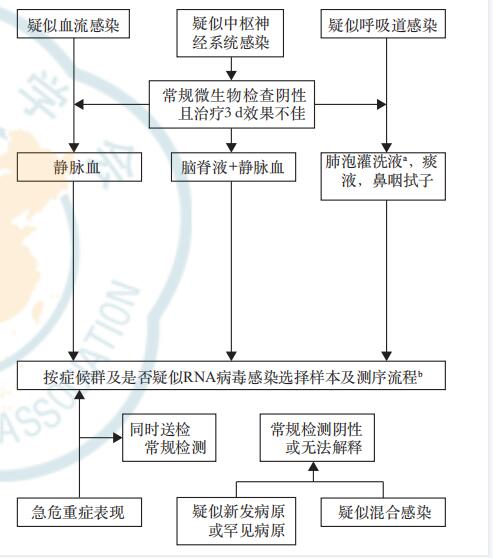
注:a呼吸道感染优先选择肺泡灌洗液,再考虑痰液和鼻咽拭子样本;b推荐 DNA 测序作为血流感染的首选检测方法,RNA 病毒感染不除外的情况推荐 RNA 测序;对于呼吸道感染,同时进行 RNA 和 DNA 测序;对于中枢神经系统感染,在排除病毒感染的情况下,优先进行 DNA 测序;当怀疑病毒感染或临床表现复杂, 无特定怀疑方向时,可同时进行RNA和DNA测序。
二、标本采集和转运
临床上采集的样本类型主要包括静脉血、脑脊液、痰液、肺泡灌洗液、胸腔积液、腹腔积液、组织、咽拭子、局灶穿刺物等。
样本采集
共识12:
各类型样本采集需要无菌操作,血液、高凝状态的胸腔积液、腹腔积液、脑脊液样本, 采集后需上下颠倒混匀5~10次。非血液标本采集通常采用带螺旋盖的无菌冻存管,但预期可能凝集的标本及血液样本需采用专用采血管。所有样本采集完成后,均需要封口膜密封,条码标记。
1、从无菌部位(如静脉血、脑脊液、胸腔积液、 腹腔积液等)采集标本时,应严格无菌操作。采集后的标本须用无菌容器盛装。
-
血液标本建议取1~3 ml(不同实验室要求不同,最低限为 0.5 ml),采用专用采血管,即游离DNA 样本保存管,采血后上下颠倒混匀5~10次;
-
脑脊液样本常规建议应为1 ml以上(新生儿因脑脊液样本较难获得,最低样本量为600 μl),采用专用采血管或无菌冻存管;
-
胸、腹腔积液需富集后提取核酸,至少采集5 ml,避免经引流管采集;
-
若增加 RNA 测序时,需提前联系实验室提供添加RNA稳定剂的采血管或无菌冻存管,在采集样本时须同时采 2 管;若样本同时进行 DNA 及 RNA 测序,1管样本量为单独DNA测序的2倍,同时向检测实验室特殊说明需立即进行核酸提取。
2、 从有菌部位(如痰液、肺泡灌洗液、咽拭子等)采集标本时,应采取必要措施,严格无菌操作等,尽量减少污染,以免干扰后续检测结果;同时标明样本的采集部位。肺泡灌洗液样本应为 3 ml 以上,采用无菌冻存管;痰液样本应为3 ml以上,采用无菌冻存管;咽拭子只适用于呼吸道病毒检测。
共识13:
推荐直接从患儿感染部位的体液或组织中采集样本。
共识14:
患儿存在感染表现但病情危重或不能耐受有创操作时,可考虑采集患儿的血液标本进行常规微生物方法检测的同时送检mNGS。
有创操作不耐受时,可送检血液标本,但可能会降低检测结果的准确性。有研究发现,对于重症肺部感染患者,痰液或肺泡灌洗液和血液标本检测病原体的一致性为40%~50%。
样本转运:所有样本均应及时送检
若样本在 24 h内到达实验室并开始检测,可考虑冰袋低温运输;若运输时间 24~72 h,应干冰运输(血液样本应先分离血浆后保存运输)。
不能及时送检样本长期保存原则 :
-
DNA 测序为-20 ℃保存不超过7 d;
-
RNA 测序应置-80 ℃理论上可长期保存;
-
避免样本反复冻融,一般不得超过 3 次;
-
若怀疑高致病性或突发传染病,严格按照国内传染病法等相关法律要求包装及转运。尽可能在医院生物安全防护条件下抽提核酸后再送测序。
三、报告解读
mNGS由于检出结果丰富,虽然提高了病原微生物检测敏感性,也对正确判读致病微生物造成了困难。建议由临床感染或临床微生物学从业人员在相关的生物信息学培训后进行解读。
共识15:
解读 mNGS 检测报告应参考检测方法的数据和检出病原序列数量、基因组覆盖度、微生物丰度等指标,结合标本采集部位、检出病原的致病特性以及患儿临床资料进行个体化解读。
共识16:
源于微生物正常定植部位的标本(例如支气管肺泡灌洗液),鉴别检出序列是属于致病微生物、污染物,还是定植菌群较为困难,应综合患儿临床表现及辅助检查综合判断。
共识17:
在新生儿群体中谨慎应用 mNGS 进行耐药基因检测。只有标本来源于无菌区(如血液、脑脊液)且标本采集过程污染概率极低时,可考虑检测耐药基因。建议检测单位选择筛选具有重要临床意义的耐药基因进行报告,意义不明确、干扰临床解读的耐药基因应慎重报告;建议临床对报告的耐药基因慎重解读,综合报告病原菌、患儿基本情况、临床药敏结果等多个因素进行判断。
圣维尔病原微生物宏基因组检测(SMPseq)采用mNGS技术对临床标本中的DNA和RNA进行高通量测序,通过与微生物参考序列数据库进行比对分析,获得疑似致病微生物的种属信息。检测范围包括基因组序列已知12818种微生物,快速、准确、全面的病原鉴定和耐药基因检测,显著提高感染病原阳性检出率,为疑难危重感染如脓毒血症,脑膜炎,重症肺炎等患者提供早期诊断和靶向用药指导,有效辅助临床决策。
文章参考来源:
中华医学会儿科学分会新生儿学组, 中华儿科杂志编辑委员会. 宏基因组二代测序技术在新生儿感染性疾病中的临床应用专家共识 [J] . 中华儿科杂志, 2022, 60(6) : 516-521.DOI:10.3760/cma.j.cn112140-20220113-00046.


 新OA系统
新OA系统 汇联易
汇联易 企业邮箱
企业邮箱 旧OA系统
旧OA系统 DTMS系统
DTMS系统 CAPA系统
CAPA系统